Modelo Atómico de Dalton

John Dalton
En 1808 Dalton formuló la teoría atómica, teoría que rompía con todas las ideas tradicionales derivada de los antiguos filósofos griegos (Demócrito, Leucipo). Esta introduce la idea de la discontinuidad de la materia, es decir, es la primera teoría científica que considera que la materia está dividida en átomos. Los postulados básicos de esta teoría son:
- La materia está dividida en unas partículas indivisibles e inalterables llamadas átomos.
- Los átomos son partículas muy pequeñas y no se pueden ver a simple vista.
- Todos los átomos de un mismo elemento son iguales entre sí, igual masa e iguales propiedades.
- Los átomos de distintos elementos tienen distinta masa y distintas propiedades.
- Los compuestos se forman cuando los átomos se unen entre sí, en una relación constante y sencilla.
- En las reacciones químicas los átomos se separan o se unen; pero ningún átomo se crea ni se destruye, y ningún átomo de un elemento se convierte en átomo de otro elemento. Esta concepción se mantuvo casi durante un siglo.
Modelo Atómico de Thomson

Joseph Thomson
Posteriormente, en el año 1897 se descubre el electrón, una de las partículas subatómicas que conforma el átomo. En 1898 Thomson propuso un modelo atómico que tomaba en cuenta la existencia de dicha partícula subatómica. Su modelo era estático, ya que suponía que los electrones estaban en reposo dentro del átomo, y que el conjunto era eléctricamente neutro.
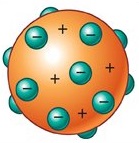
El modelo de Thomson era parecido a un pastel de frutas: los electrones estaban incrustados en una masa esférica de carga positiva. La carga negativa total de los electrones era la misma que la carga total positiva de la esfera, por lo que dedujo que el átomo era neutro.
Thomson también explicó la formación de iones, tanto positivos como negativos. Cuando el átomo pierde algún electrón, la estructura queda positiva y se forman iones positivos; pero si el átomo gana algún electrón, la estructura queda negativa y se forman iones negativos.
Modelo Atómico de Rutherford

Ernest Rutherford
Tras el descubrimiento del Protón, Rutherford formuló su modelo atómico. En 1911, Rutherford empleó las partículas alfa para determinar la estructura interna de la materia.
Ernest Rutherford, que estudio con Thomson en la Universidad de Cambridge, utilizó partículas alfa para demostrar la estructura de los átomos. Junto con su colega Hans Geiger y un estudiante de licenciatura llamado Ernest Marsden. Rutherford efectuó una serie de experimentos utilizando láminas muy delgadas de oro y de otros metales, como blanco de partículas a provenientes de una fuente radiactiva. Ellos observaron que la mayoría de las partículas atravesaban la lámina sin desviarse, o bien con una ligera desviación. De vez en cuando, algunas partículas alfa eran dispersadas (o desviadas) de su trayectoria con un gran ángulo. En algunos casos, las partículas alfa regresaban por la misma trayectoria hacia la fuente radiactiva
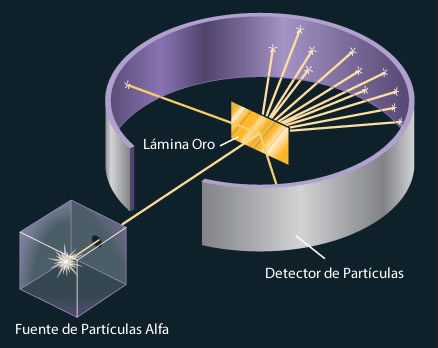
Diseño experimental de Rutherford para medir la dispersión de las partículas alfa causada por una lámina de oro. La mayoría de las partículas alfa atraviesan la lámina de oro con poca o ninguna desviación. Algunas se desvían con un ángulo grande ocasionalmente alguna partícula invierte su trayectoria.
A partir de ese experimento dedujo que:
- La mayoría de las partículas atraviesan la lámina sin desviarse (99,9%).
- Algunas partículas se desvían (0,1%).
Al ver que no se cumplía el modelo propuesto por Thomson, Rutherford formuló el modelo nuclear del átomo. Según este modelo, el átomo está formado por un núcleo y una corteza:
- En el núcleo se concentra casi la totalidad de la masa del átomo, y tiene carga positiva.
- La corteza está formada por los electrones, que giran alrededor del núcleo describiendo órbitas circulares (sistema solar en miniatura)
Así mismo, también dijo que la materia es neutra, ya que la carga positiva del núcleo y la negativa de la corteza se neutralizan entre sí.
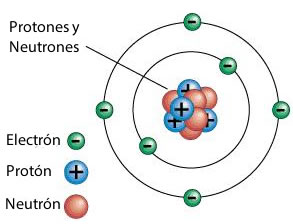
Modelo Atómico de Rutherford
Rutherford dedujo que:
La materia está casi vacía; el núcleo es 100.000 veces más pequeño que el radio del átomo. La mayoría de las partículas alfa no se desvían porque pasan por la corteza, y no por el núcleo. Las que pasan cerca del núcleo se desvían porque son repelidas. Cuando el átomo suelta electrones, el átomo se queda con carga negativa, convirtiéndose en un ión negativo; pero si, por el contrario, el átomo gana electrones, la estructura será positiva y el átomo se convertirá en un ión negativo. El átomo es estable.
Modelo Atómico de Böhr

Niels Böhr
Tras el descubrimiento del neutrón, en 1913 Böhr intentó mejorar el modelo atómico de Rutherford aplicando las ideas cuánticas de Planck a su modelo. Para realizar su modelo atómico se valió del átomo de hidrógeno; describió el átomo de hidrógeno con un protón como núcleo y con un electrón girando a su alrededor. Las nuevas ideas sobre la cuantización de la energía son las siguientes:
- El átomo está cuantizado, ya que solo puede poseer unas pocas y determinadas energías.
- El electrón gira en unas órbitas circulares alrededor del núcleo, y cada órbita es un estado estacionario que va asociado a un numero natural, “n” (núm. cuántico principal), y toma valores del 1 al 7. Así mismo, cada nivel “n” está formado por distintos subniveles, “l”. Y a su vez, éstos se desdoblan en otros (efecto Zeeman), “m”. Y por último, hay un cuarto número cuántico que se refiere al sentido, “s”. Los niveles de energía permitidos son múltiplos de la constante de planck.
- Cuando un electrón pasa de un nivel de energía a otro, se absorbe o se emite energía.
- Cuando el electrón está en n=1 se dice que está en el nivel fundamental (nivel de mínima energía); al cambiar de nivel el electrón absorbe energía y pasa a llamarse electrón excitado.
Böhr situó a los electrones en lugares exactos del espacio. Es el modelo planetario de Böhr.
Modelo Mecano – Cuántico
Es el modelo actual; fue expuesto en 1925 por Heisenberg y Schrödinger.

Erwin Schrödinger

Werner Heisenberg
Aspectos característicos:
- Dualidad onda-partícula: Broglie propuso que las partículas materiales tienen propiedades ondulatorias, y que toda partícula en movimiento lleva una onda asociada.
- Principio de indeterminación: Heisenberg dijo que era imposible situar a un electrón en un punto exacto del espacio. Las ecuaciones del modelo mecano-cuántico describen el comportamiento de los electrones dentro del átomo, y recogen su carácter ondulatorio y la imposibilidad de predecir sus trayectorias exactas. Así establecieron el concepto de orbital, región del espacio del átomo donde la probabilidad de encontrar un electrón es muy grande.
- Características de los orbitales: La energía está cuantizada. Lo que marca la diferencia con el modelo de Böhr es que este modelo no determina la posición exacta del electrón, sino la mayor o menor probabilidad. Dentro del átomo, el electrón se interpreta como una nube de carga negativa, y dentro de esta nube, en el lugar en el que la densidad sea mayor, la probabilidad de encontrar un electrón también será mayor.
- El comportamiento de los electrones dentro del átomo se describe a través de los números cuánticos. Los números cuánticos se encargan del comportamiento de los electrones, y la configuración electrónica de su distribución. Y por último, dada la cantidad de elementos, se necesitaba una clasificación. Hoy en día se utiliza la Tabla Periódica, aunque le precedieron muchos otras propuestas. En la Tabla Periódica los elementos se clasifican según el número atómico.

